โดย …ดร. วีระณีย์ ทองศรี
ภาควิชาโรคพืช คณะเกษตร มหาวิทยาลัยเกษตรศาสตร์ กรุงเทพฯ 10900 โทร. 025790113 ต่อ 1294
ในปัจจุบันการผลิตไม้ผลทั้งในและต่างประเทศได้มุ่งเน้นให้มีระบบการผลิตเพื่อให้ได้ผลิตผลที่มีความปลอดภัยต่อทั้งผู้ผลิต ผู้บริโภค และสิ่งแวดล้อม ระบบการปลูกไม้ผลแบบปลอดสารพิษจึงถูกส่งเสริมให้มีการปฏิบัติในวงกว้าง ด้วยเหตุนี้การจัดการโรคพืชโดยชีววิธีจึงเป็นวิธีการหนึ่งที่มีวัตถุประสงค์เพื่อทดแทนหรือลดปริมาณการใช้สารเคมี ให้น้อยลงโดยใช้จุลินทรีย์ปฏิปักษ์เป็นตัวควบคุมโรค (biocontrol agents)ซึ่งในปัจจุบันมีรายงานการวิจัยเกี่ยวกับการนำเชื้อจุลินทรีย์หลายๆ ชนิดมาใช้ควบคุมโรคทั้งก่อนและหลังการเก็บเกี่ยวของไม้ผลอย่างกว้างขวาง แต่มีจุลินทรีย์เพียงไม่กี่ชนิดเท่านั้นที่มีประสิทธิภาพสูงในการควบคุมโรคพืช และในหลายประเทศได้มีการพัฒนาจุลินทรีย์เหล่านี้ซึ่งมีทั้งเชื้อรา แบคทีเรีย และยีสต์ให้เป็นชีวผลิตภัณฑ์เพื่อเพิ่มประสิทธิภาพในการควบคุมโรคพืชให้ดียิ่งขึ้น เช่น BiosaveTM (Pseudomonas syringae สหรัฐอเมริกา) ShemerTM (Metschnikowia fructicola แอนติกัว-บาร์บิวด้า) CandifruitTM (Candida sake CPA-1 สเปน) PantovitalTM (Pantoea agglomerans สเปน) SerenadeTM (Bacillus subtilis สหรัฐอเมริกา) BoniprotectTM (Aureobasidium pullulans เยอรมัน) และ TrisanTM(Trichoderma harzianum ไทย) ซึ่ง Canamas et al. (2011) กล่าวว่าการใช้ผลิตภัณฑ์จากเชื้อแบคทีเรีย Pantoea agglomerans ในแปลงปลูกส้มสามารถลดการเกิดโรคผลเน่า (green mold) ซึ่งมีสาเหตุจากเชื้อรา Penicillium digitatum ได้ดีกว่าการใช้เชื้อจุลินทรีย์สด โดยกลไกในการเข้าทำลายเชื้อสาเหตุโรคพืชของจุลินทรีย์ปฏิปักษ์มีหลายรูปแบบดังนี้คือ การเป็นปรสิต (parasitism) การสร้างสารปฏิชีวนะ (antibiosis) การผลิตเอนไซม์ย่อยผนังเซลล์ของเชื้อโรคพืช (production of cell wall degrading enzymes) การแข่งขันเพื่อครอบครองพื้นที่และอาหาร (competition for nutrients and space) และการชักนำให้พืชมีความต้านทานโรค (induction of disease resistance in plant) ซึ่งเชื้อจุลินทรีย์เหล่านี้มักมีหลายกลไกร่วมกันในการควบคุมโรคพืช
เชื้อจุลินทรีย์ที่นำมาใช้ในการควบคุมโรคของไม้ผลนี้ ส่วนมากนักวิจัยมุ่งคัดเลือกหาเชื้อที่ไม่ก่อให้เกิดโรคกับพืชจากบริเวณในส่วนผิวของผลทั้งในช่วงก่อนเก็บเกี่ยวและขณะเก็บรักษา เนื่องจากจุลินทรีย์ที่เป็นประโยชน์เหล่านี้มักพบเป็นจำนวนมากในบริเวณผิวเปลือกของผล (Manso and Nunes, 2011) หรืออาจพบมากในบริเวณผิวใบ (Janisiewicz and Korsten, 2002) อย่างไรก็ตามการใช้จุลินทรีย์ควบคุมโรคของไม้ผลมักจะต้องใช้จุลินทรีย์ที่มีความเข้มข้นสูง แต่ประสิทธิภาพในการควบคุมโรคยังไม่ดีเท่ากับการใช้สารเคมีเมื่อมีการใช้จุลินทรีย์เดี่ยวๆ (Cao et al., 2011) ดังนั้นการผลิตจุลินทรีย์ในการควบคุมโรคพืชจึงยังต้องมีการพัฒนาเพื่อให้มีรูปแบบที่เหมาะสมต่อการนำไปใช้และเพิ่มขีดความสามารถในการควบคุมโรคให้สูงขึ้น
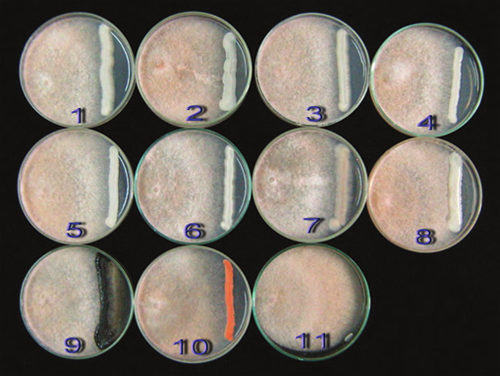
ภาพที่ 1 การทดสอบเชื้อยีสต์ 10 ชนิดในการเป็นจุลินทรีย์ปฏิปิกษ์ต่อการเจริญของเชื้อรา Colletotrichum musae สาเหตุโรคแอนแทรคโนสของกล้วยหอมทองบนจานอาหารเลี้ยงเชื้อ potato dextrose agar โดยวิธี dual culture ที่อายุ 7 วัน โดยที่ 1 = Candida guilliermondii 2 = Candida utilis 3 = Candida sake 4 = Saccharomycopsis fibuligera 5 = Pichia membranaefaciens 6 = Candida tropicalis 7 = Debaryomyces hanseni 8 = Cryptococcus humicola 9 = Aureobasidium pullulans 10 = Rodotorula glutinis 11 = Control
การควบคุมโรคหลังการเก็บเกี่ยวของไม้ผลจะประสบผลสำเร็จหรือไม่นั้นขึ้นอยู่กับการจัดการโรคตั้งแต่ในแปลงปลูก โดยจุลินทรีย์ที่ถูกนำมาใช้ในการจัดการโรคในสภาพไร่นี้ควรจะทำให้อยู่ในรูปแบบของผลิตภัณฑ์เพื่อช่วยส่งเสริมการมีชีวิตรอดของจุลินทรีย์ที่เป็นประโยชน์ให้ทนต่อสภาพแวดล้อมได้ยาวนานขึ้น หรือถ้าหากเป็นเชื้อจุลินทรีย์สดก็มักมีการใช้ร่วมกับตัวควบคุมอื่นๆ เพื่อเพิ่มประสิทธิภาพในการควบคุมโรคให้ดียิ่งขึ้น เช่น การใช้เชื้อแบคทีเรีย Pseudomonas solanacearum Pf1 ร่วมกับสารสกัดจากพืชควบคุมโรคเหี่ยวของกล้วยที่เกิดจากเชื้อรา Fusarium oxysporum f.sp. cubense (Akila et al., 2011) การใช้เชื้อรา Trichoderma harzianum ร่วมกับ mycorrhiza ช่วยลดการเกิดโรคเหี่ยวของแตงซึ่งเกิดจากเชื้อรา F. oxysporum f.sp. melonis (Martinez-Medina et al., 2011) และการใช้เชื้อยีสต์ Candida sake CPA-1 ร่วมกับสารเคลือบผิวฉีดพ่นแปลงองุ่นช่วยลดการเกิดโรคผลเน่า (gray mold) ที่มีสาเหตุจากเชื้อรา Botrytis cinerea ภายหลังการเก็บเกี่ยวได้ดีกว่าการใช้เชื้อยีสต์อย่างเดียว ทั้งนี้เนื่องจากสารเคลือบผิวมีประสิทธิภาพในการช่วยให้เชื้อยีสต์มีความคงทนและมีชีวิตรอดได้นานขึ้น (Canamas et al., 2011) นอกจากนั้น Hasham and Abo-Elyousr (2011) ได้นำเชื้อจุลินทรีย์ ปฏิปักษ์หลายชนิดมาใช้ร่วมกันในการควบคุมโรครากปมจากไส้เดือนฝอย Meloidogyne incognita ของมะเขือเทศรับประทานสด ได้แก่ เชื้อแบคทีเรีย Pseudomonas fluorescens เชื้อรา Paecilomyces lilacinus เชื้อยีสต์ Pichia guilliermondii และไซยาโนแบคทีเรีย Calothrix parietin พบว่าสามารถลดขนาดของปมให้เล็กลงกว่าการใช้จุลินทรีย์เพียงชนิดเดียว รวมทั้งจุลินทรีย์ดังกล่าวมีคุณสมบัติในการส่งเสริมการเจริญเติบโตของพืชและชักนำให้พืชเกิดความต้านทานต่อโรค อย่างไรก็ตาม การใช้จุลินทรีย์ควบคุมโรคพืชในแปลงปลูกจะต้องคำนึงถึงสภาพแวดล้อมให้มีความเหมาะสมต่อการเจริญเติบโต และการขยายพันธุ์ของจุลินทรีย์เหล่านี้ โดยเฉพาะการหว่านลงดินจะต้องมีการปรับสภาพดินให้มีความอุดมสมบูรณ์อยู่เสมอ และควรมีการปรับความเป็นกรดด่างของดินให้เหมาะสมต่อการเจริญเติบโตของเชื้อจุลินทรีย์ชนิดนั้นๆ

ภาพที่ 2 การใช้เซลล์แขวนลอยของเชื้อยีสต์ Candida sake C. utilis Debaryomyces hansenii และ Aureobasidium pullulans ในการควบคุมการเกิดโรคแอนแทรคโนสที่เกิดจากเชื้อรา Colletotrichum musae บนกล้วยหอมโดยวิธีทำแผล
สำหรับการใช้จุลินทรีย์ควบคุมโรคภายหลังการเก็บเกี่ยวของผลไม้ ส่วนมากนิยมใช้เชื้อยีสต์และแบคทีเรียเป็นตัวควบคุมโรคมากกว่าเชื้อรา เนื่องจากนักวิจัยส่วนใหญ่ค่อนข้างมั่นใจว่ามีเชื้อยีสต์หลายชนิดที่ไม่ทำลายเนื้อเยื่อพืชหรือไม่ทำให้พืชเป็โรค (Lima et al. 1997) รวมทั้งไม่สร้างสารพิษและมีคุณสมบัติในการแก่งแย่งอาหารได้ดี ซึ่งเชื้อยีสต์ที่มีการนำมาใช้ในการควบคุมโรคหลังการเก็บเกี่ยวของผลิตผลมีหลายชนิด ได้แก่ Candida spp. Cryptococcus spp. Debaryomyces spp. Endomycopsis spp. Pichia spp. Aureobasidium pullulans Saccharomycopsis fibuligera Rhodosporidium spp.และ Rhodotorula glutinis ส่วนเชื้อแบคทีเรียก็มีสายพันธุ์เฉพาะเจาะจงที่ไม่ก่อให้เกิดโรคกับพืช พร้อมกับมีคุณสมบัติในการยับยั้งโรค ซึ่งส่วนมากจัดอยู่ในสกุล Pseudomonas และ Bacillus จึงค่อนข้างมีความปลอดภัยในการที่จะนำเชื้อจุลินทรีย์เหล่านี้มาใช้กับผลิตผลหลังการเก็บเกี่ยวเพื่อรอการบริโภค จุลินทรีย์ที่นำมาใช้ควบคุมโรคหลังการเก็บเกี่ยวมักใช้ร่วมกับตัวควบคุมชนิดอื่นๆ หรือวิธีการอื่นๆ เพื่อเพิ่มศักยภาพในการควบคุมโรคให้สูงขึ้น เช่น ใช้ร่วมกับการจุ่มน้ำร้อนหรือจุ่มในสารเคมีที่ระดับความเข้มข้นต่ำๆ โดยพบว่าการฉีดพ่นผลกล้วยด้วยเชื้อยีสต์แล้วตามด้วยการจุ่มในน้ำร้อนที่อุณหภูมิ 50 องศาเซลเซียสเป็นเวลา 20 นาที หรือจุ่มในสารเคมีไธอะเบนดาโซล 150 ppm สามารถช่วยลดการเกิดโรคขั้วหวีเน่าได้อย่างสมบูรณ์ (Sangchote and Sangwanich, 2005) นอกจากนั้นการใช้จุลินทรีย์ร่วมกับการเก็บรักษาไว้ในสภาพบรรยากาศดัดแปลงก็เป็นวิธีการหนึ่งที่มีประสิทธิภาพในการควบคุมโรคเช่นเดียวกัน ดังเช่นการเก็บผลท้อที่ผ่านการจุ่มในเซลล์แขวนลอยของเชื้อแบคทีเรีย Bacillus amyloliquefaciens ไว้ในถุงพลาสติกที่ย่อยสลายได้ที่อุณหภูมิ 4 องศาเซลเซียส พบการเกิดโรคผลเน่าน้อยที่สุดเมื่อเปรียบเทียบกับการใช้เชื้อแบคทีเรียอย่างเดียว (Arrebola et al., 2010) หรือการใช้จุลินทรีย์ร่วมกับสารเติมแต่งอาหาร (food additives) ดังที่พบจากการใช์เชื้อยีสต์ Aureobasidium pullulans ร่วมกับแคลเซียมคลอไรด์หรือโซเดียมไบคาร์บอเนตช่วยลดการเกิดโรคผลเน่าของเชอรี่ที่มีสาเหตุจากเชื้อรา B. cinerea ได้ดีที่สุด (Ippolito et al., 2005) ตลอดจนการใช้เชื้อจุลินทรีย์ปฏิปักษ์ร่วมกับจุลินทรีย์ชนิดอื่น เช่น ยีสต์ Cryptococcus laurentii ใช้ร่วมกับเชื้อรา Lentinula edodes สามารถลดการเกิดโรคผลเน่าซึ่งเกิดจากเชื้อรา Penicillium expansum บนผลแอปเปิลได้ดีกว่าการใช้เชื้อยีสต์อย่างเดียว (Tolaini et al. 2010) นอกจากนั้น เชื้อจุลินทรีย์ปฏิปักษ์ยังมีคุณสมบัติในการช่วยลดการปนเปื้อนของสารพิษในผลิตผล เช่นที่พบในผลแอปเปิลที่ถูกเข้าทำลายโดยเชื้อรา P. expansum เนื่องจากจุลินทรีย์ปฏิปักษ์มีกลไกในการยับยั้งการสร้างสารพิษของเชื้อราดังกล่าวได้ (Tolaini et al., 2010)
จะเห็นได้ว่าการควบคุมโรคของไม้ผลโดยใช้จุลินทรีย์ปฏิปักษ์เพื่อการควบคุมโรคทั้งก่อนและหลังการเก็บเกี่ยว มักจะต้องใช้ร่วมกับกรรมวิธีอื่นๆ จึงจะทำให้การควบคุมโรคอยู่ในระดับที่เป็นที่น่าพอใจ และจะต้องมีวิธีการใช้ที่เหมาะสม อย่างไรก็ตาม การพัฒนาผลิตภัณฑ์จากจุลินทรีย์เหล่านี้ก็ยังไม่หยุดนิ่ง เนื่องจากนักวิจัยจะต้องสรรหาวิธีการเพื่อให้เชื้อจุลินทรีย์ปฏิปักษ์มีความคงทนต่อสภาพแวดล้อมและเพิ่มศักยภาพในการควบคุมโรคเพื่อให้เกิดประโยชน์สูงสุดจากการใช้จุลินทรีย์เหล่านี้
เอกสารอ้างอิง
- Akila, R., L. Rajendran, S. Harish, K. Saveetha, T. Raguchander and R. Samiyappan. 2011. Combined application of botanical formulations and biocontrol agents for the management of Fusarium oxysporum f. sp. cubense (Foc)causing Fusarium wilt in banana. Biological Control 57: 175–183.
- Arrebola, E., D. Sivakumar, R. Bacigalupo and L. Korsten. 2010. Combined application of antagonist Bacillus amyloliquefaciens and essential oils for the control of peach postharvest diseases. Crop Protection 29: 369–377.
- Canamas,T.P., I. Vinas, J. Usall, C. Casals, C. Solsona and N. Teixido. 2011. Control of postharvest diseases on citrus fruit by preharvest application of the biocontrol agent Pantoea agglomerans CPA-2. Part I. Study of different formulation strategies to improve survival of cells in unfavourable environmental conditions. Postharvest Biology and Technology 49: 86–95.
- Cao, S., Z. Yang, Z. Hua and Y. Zheng. 2011. The effects of the combination of Pichia membranefaciens and BTH on controlling of blue mould decay caused by Penicillium expansum in peach fruit. Food Chemistry 124: 991-996. De Cal, A., C. Redondo, A. Sztejnberg and P. Melgarejo. Biocontrol of powdery mildew by Penicillium oxalicum in open-field nurseries of strawberries. Biological Control 47: 103–107.
- Hashem, M. and K.A. Abo-Elyousr. 2011. Management of the root-knot nematode Meloidogyne incognita on tomato with combinations of different biocontrol organisms. Crop Protection 30: 285-292.
- Ippolito, A., L. Schena, I. Pentimone and F. Nigro. 2005. Control of postharvest rots of sweet cherries by pre- and postharvest applications of Aureobasidium pullulans in combination with calcium chloride or sodium bicarbonate. Postharvest Biology and Technology 36: 245–252.
- Janisiewicz, W.J. and L. Korsten. 2002. Biological control of postharvest diseases of fruit. Annual Review of Phytopathology 40: 411-441.
- Lima G., A. Ippolito, A. Nigro and M. Salerno. 1997. Effectiveness of Aureobasidium pullulans and Candida oleophila against postharvest strawberry rots. Postharvest Biology and Technology 10: 169-178.
- Manso, T. and C. Nunes. 2011. Metschnikowia andauensis as a new biocontrol agent of fruit postharvest diseases. Postharvest Biology and Technology 61: 64–71.
- Martiํnez-Medina, A., A. Roldan and J. A. Pascual. 2011. Interaction between arbuscular mycorrhizal fungi and Trichoderma harzianum under conventional and low input fertilization field condition in melon crops: Growth response and Fusarium wilt biocontrol. Applied Soil Ecology 47: 98-105.
- Sangchote S. and S. Sangwanich. 2005. Selection and screening antagonistic yeasts to control crown rot of banana cv. Kluai Hom Thong, caused by Lasiodiplodia theobromae. Proceedings of 43rd Kasetsart University Annual Conference. 1-4 February 2005. p 86-94.
- Tolaini , V., S. Zjalic, M. Reverberi, C. Fanelli, A. A. Fabbri, A. Del Fiore, P. De Rossi and A. Ricelli. 2010. Lentinula edodesenhances the biocontrol activity of Cryptococcus laurentii against Penicillium expansum contamination and patulin production in apple fruits. International Journal of Food Microbiology 138: 243–249.



